患者|急性肾损伤(AKI)的管理(2018文献建议)
AKI的管理包括优化液体状态、避免肾损伤药物 。 对于大多数病人来说 , 使用晶体液优于胶体液 , 尽量避免使用羟乙基淀粉 。 液体过负荷在AKI患者当中是和不良预后密切相关的 , 应当避免极力避免 。 目前没有药物能够治疗AKI 。 最佳的肾脏替代时机目前仍是未知的 , 目前关于这些的研究较为火热 。 最近有文献报道 , AKI不是一个自陷的疾病 , 而是和慢性肾病风险增加、持续肾损伤、肾衰竭密切相关的 。
AKI的诊断和评估
当肾功能降低的时候 , 体内的肌酐、尿素氮、和其他一些无法测量的代谢废物堆积 , 引起一系列的病理生理改变 , 这就是AKI 。 最近 , 已经使用损伤来替代衰竭来描述肾功能的发展过程 , 这是因为尽管轻度的肾损伤也可能和极差的预后相关 。 AKI非常常见 , 大概5-10%的住院病人会出现AKI , ICU患者中这部分比例可高达60% 。 引起AKI的因素有很多 , 它不应当被当作是一个单独的疾病 。 对于AKI来说 , 尽管一些管理方案是通用的 , 但是有一些对于特定情况 , 管理方案还是不同的 。 当AKI出现的时候 , 首要的任务就是尽快明确AKI的病因 , 对于造成肾损伤可逆性因素需要额外注意 。
早期AKI阶段的表现可以是异质的 , 在过去十多年 ,, 很多流行病学研究和临床试验对AKI进行了观察 , 想要弄清楚AKI的情况 。 在2012年 , KDIGO组织从初始定义上明确了AKI的几个因素 。 AKI分期是基于尿量和血清肌酐水平的 。 如果尿量和肌酐不匹配 , 使用最为严重的那个指标作为分期标准 。 尿量是一个重要的评判不良预后的指标 , 但是它的病理生理意义仍然有争议 。 通过KDIGO中的尿量标准来定义肾损伤 , 不管肌酐水平 , 这一部分病人容易出现液体过负荷 , 因为危重病人的摄入通常来讲是很多的 。
图示:不同AKI标准
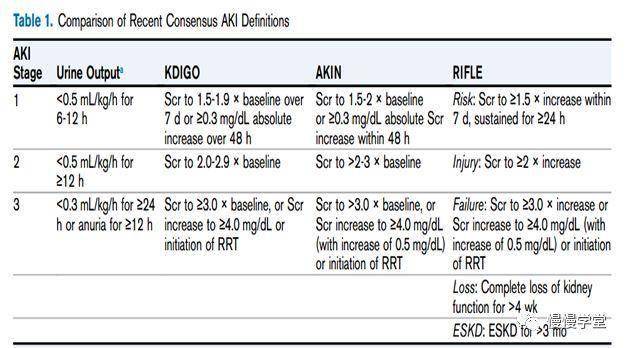
文章图片
1mg/dl肌酐=88.4umol/l , 4mg/dl=353.6umol/l;0.5mg/l=44.2umol/l
目前来讲 , 肾小球滤过率尽管只能反映肾功能众多情况当中的一个 , 但它仍是急性或慢性肾脏病变的重要指标 。 临床上很少能够直接测量肾小球滤过率 , 一般都是使用一些替代指标 。 有一些肾小球滤过率的估算公式(比如Cockcroft-Gault, MDRD Study, and CKD-EPI) , 但是如果患者肌酐水平波动较大 , 这些公式意义不大 。 在肌酐波动较大的时候 , 公式可以用来评判动态的肾小球滤过率 , 但是目前这方面的应用尚未被广泛证实 。 在严重的AKI当中(比如少尿患者) , 应当认为患者肾小球滤过率小于10ml/min 。
肌酐的变化可以在肾功能恶化之后 , 因此当前肌酐水平并不一定能够反映出当前的肾功能 。 严重疾病的时候或者肌肉病变的时候 , 可以引起肌酐生成减少 , 或者液体复苏时候肌酐浓度会被稀释 , 这些都使得肾功能的评估更加困难 。 胱抑素C目前被用作肾小球滤过率的评估指标 , 在肾小球滤过率较高和肌肉减少的患者中准确性更高 。 但是 , 没有指导分期的作用 , 液体复苏对胱抑素C的影响情况也未知 。 临床上最好是能直接测量患者的肾小球滤过率 , 但目前并没有适用的方法 。
肾小管坏死标志物包括NGAL、KIM-1、IL-8、L-FABP等 。 未来AKI的定义可能会包括合适的生物标志物 。 有一些标志物能够反映肾脏的压力 , 比如TIMP-2、IGFBP-7.目前已经被美国FDA批准用于评估KDIGO2级到3级的危险因素 。 目前这些标志物的研究发展很迅速 , 临床应用在广泛推广 。
AKI病因分析
对AKI患者应当进行病因分析 , 以便及时治疗 。 病史采集、病史回顾、体格检查是基本工作 。 比如 , 一个心脏搭桥术后的患者 , AKI的发生可能是搭桥手术问题 , 可能是低血容量 , 也可能是术后心肌问题或感染性休克、胆固醇栓塞 。 为了明确病因 , 仔细的评估是必须的 , 同时也要进行体格检查、实验室检查(网状瘀斑、外周嗜酸性粒细胞增多可能是胆固醇堆积问题) 。
所有的AKI患者都应当进行血流动力学和容量状态的评估 , 使用一些可视化的体征或体格检查;危重病人 , 比如说休克的病人 , 能够从有创血流动力学当中获益(动脉血压监测 , 中心静脉压监测或心输出量监测) 。 尿钠排泄指数也有一定的诊断作用 。 但是 , 危重病人使用这些指数受到很大的限制 , 因为患者可能肾性、肾前性少尿因素都存在 。 尿显微镜检查发现肾小管坏死和颗粒管型对于诊断急性肾小管坏死有一定的帮助 , 急性肾小管坏死是AKI的主要原因 。 但是肾活检发现肾小管坏死轻微或者没有严重的细胞坏死 , 因此肾小管坏死这个词语有点用词不当 。 急性肾小管坏死可以用来描述AKI的特异性和严重程度 , 而不能当作疾病本身的病理生理改变 。
图示:肾损伤的原因分析

文章图片
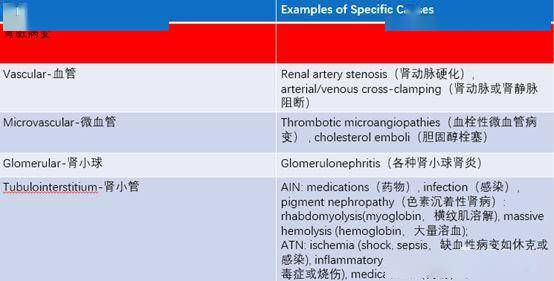
文章图片
怀疑患有可医治的肾内病变引起的AKI , 比如急性间质性肾炎、肾小球肾炎、血栓性微血管病 , 这些病人应当进行尿沉积检查和血液相关的检查 。 当有新发的蛋白尿(尿蛋白大于3g/d)、血尿、尿沉积、明显的肾灌注减少、梗阻、急性肾小管坏死的时候 , 应当进行肾活检 。 一项回顾性的研究发现 , 肾活检发现51%的AKI病人具有特异性的病因 , 这在很大程度上影响治疗 。 然而肾活检有一些并发症 , 其中最常见的就是出血 。
临床上急性间质性肾炎(AIN)很可能不被诊断;抗生素和质子泵抑制剂的广泛使用使AIN很常见 。 当不合并有皮疹或嗜酸性粒细胞增多等全身症状的时候 , AIN很难被诊断出来 。 尿嗜酸性粒细胞特异性很差 , 肾活检是唯一的明确诊断的方法 。 AIN的治疗包括终止引起肾损伤的药物和激素疗法 。
在怀疑梗阻性病变的时候 , 可以进行肾脏超声或腹部CT、盆腔CT(无需造影剂)检查 。 对于双肾患者 , 要想引起AKI , 必须有两侧梗阻 。 对于有明确病因的AKI患者 , 常规的检查不一定是必须的 。
AKI的管理
AKI的患者应当进行肾功能的监测 , 比如监测肌酐浓度和尿量 , 谨慎评估容量和血流动力学状态 , 使用补液、利尿剂或其他血流动力学支持来进行治疗 。
肾毒性药物应当避免使用 , 改为肾毒性小的药物 。 药物引起的肾毒性应当被重视 , 在儿童用药当中 , 这种认知能够降低肾毒性药物或氨基糖苷药物的使用 , 降低AKI的发生率 。 此外 , 肾小球滤过率降低的时候 , 尤其是分期达到2级或3级的时候 , 药物代谢减慢 , 药物血药浓度会增加 , 这种情况下 , 药物用量应当减少或避免使用肾脏代谢的药物;钆本身不是药物 , 但它却能诱发肾系统纤维变性、皮肤或其他器官硬化 , 引起死亡 。 尽管发生率很低 , 在使用过程中应当权衡利弊 。
至于特异点肾毒性药物 , 目前万古霉素是研究热点 。 在治疗严重的MRSA感染的时候 , 需要较高的万古霉素谷浓度 , 如果合并肾功能不全 , 谷浓度可以达到非常高的水平(>50ug/ml) 。 哌拉西林他唑巴坦能够加重万古霉素的肾毒性 , 但是机制不明 。 非甾体类抗炎药和ACEI或ARB类降压药物在AKI的时候应当被终止使用 。 尽管目前研究不在支持碘造影剂和肾脏损伤密切相关 , 但是对于AKI高危的病人来说 , 还是需要尽量避免使用碘造影剂 。
图示:肾毒性药物

文章图片

文章图片
目前有研究想使用集束化方案来治疗AKI , 提高AKI的生活质量 。 将276个心脏术后合并肾功能损伤生物标记为升高的病人分为常规治疗组和严格集束化治疗组(治疗依照KDIGO指南) , 发现集束化治疗组AKI发生率明显降低 。 生物标志物升高的患者很容易出现AKI , 提前干预能够降低AKI的发生 。 但是仍然需要进一步去研究制定这种集束化治疗的内涵 。
对AKI患者进行血流动力学管理 , 尤其是那些休克的病人 , 是非常重要的 。 在正常情况下 , 肾脏血流因为自我调节功能 , 尽管血液变化 , 肾血流可以不变 , 但AKI患者当中这种自我调整功能紊乱 。 液体滴定和血管活性药物可能会很复杂:低血压能够导致持续的肾损伤 , 但是在容量不足的情况下给予血管活性药物会减少肾血流 。 同时 , AKI患者更容易出现容量过负荷 , 血管内液体供应过度会引起肾损伤 。
液体复苏
目前没有液体治疗和安慰剂治疗相对比治疗AKI的临床研究 , 但是可以认为 , 对于那些肾血流不足的病人来说 , 如果液体复苏能够增加心输出量 , 肾脏也会跟着获益 。 目前有研究证实EGDT对于病死率和CRRT需求没有帮助 。 尽管早期给予液体复苏对于那些感染性休克的患者是有益的 , 但是液体过负荷 , 尤其是感染性休克后期 , 是有害的 。 已经有数个研究发现液体正平衡和病死率密切相关 。
目前有很多方法可以评估液体反应性 , 众多方法无法相互替代 。 我们推荐使用多种方法联合的方式来明确患者液体状态 , 病情需要持续、反复评估患者的液体反应性 。 对于AKI没有容量反应性的那些患者来说 , 静脉补液应当谨慎 。 在有效的液体复苏之后 , 尽管病人有容量反应性、有容量依赖 , 血管活性药物也应当使用以避免液体过负荷 。 在目前研究下 , 液体复苏的液体选择没有明确推荐 。
白蛋白、羟乙基淡粉、明胶等胶体通过提高胶体渗透压 , 扩大渗透梯度 , 使晶体液在血管内外重新平衡 , 从而增加血管内容量 。 炎症反应的病人血管渗透性增加 , 这种效果可能不显著 。
白蛋白很贵 , 但是相对来说是安全的 , 是液体复苏的一个重要选择 。 在一项研究中发现 , 4%的白蛋白没有肾脏保护作用 , 不改善病死率 , 但是能够减少液体的使用量 。 在特殊疾病当中 , 比如说肝硬化患者 , 白蛋白能够减少液体的使用 , 可以当作一种选择 。 终末期肝病患者当中 , 白蛋白有明确的指征 , 它能够降低AKI的风险 。 对于创伤性脑损伤的患者来说 , 白蛋白的使用应当被避免 , 因为它可能会增加死亡风险 。
羟乙基淀粉种类较多 , 有不同的分子量、分子替换、强度等 , 都比蛋白要便宜 。 有研究发现羟乙基淀粉能够使近端小管空泡形成、细胞水肿 , 从而造成肾损伤 。 有一些改良的羟乙基淀粉肾毒性较小 。 CHEST研究发现 , 使用6%的羟乙基淀粉增加了CRRT的比例 。 这项研究同时挑战了RIFLE关于使用尿量联合肌酐来对AKI分级的规定:大量的AKI的分级是通过尿量来进行的 。 羟乙基淀粉组的患者AKI发生率较低 , 但严重程度更大 , 需要CRRT比例更高 。 这项研究发布后 , 美国FDA在羟乙基淀粉的包装当中加入了新的警示提醒 。
其他的合成胶体就是明胶了 , 目前关于明胶和AKI的研究数据较少 。 整体来说 , 目前胶体使用缺乏明确的益处 , 因此常规使用胶体补液扩容应当被禁止 。
在低血容量患者当中胶体使用很吸引人 。 CRISTAL研究发现 , 在多中心研究中 , 低血容量休克患者液体复苏 , 45%的胶体使用的是羟乙基淀粉 , 这种治疗并没有增加28天病死率和CRRT的几率 , 但是90天病死率是下降的 , 机械通气的比例也较低 , 血管活性药物的使用也较少 。 因此 , 胶体的使用需要把握时机 , 目前没有数据支持常规使用胶体作为液体复苏的液体选择 。
【患者|急性肾损伤(AKI)的管理(2018文献建议)】钠盐
0.9%的生理盐水氯离子含量高于细胞外液 , 接受生理盐水的患者容易出现高氯性代谢性酸中毒 。 高氯血症能够增加肾脏血管阻力 , 增加肾素活性 , 降低肾小球滤过率 。 在正常志愿者中 , 和使用平衡液对比 , 使用0.9%的生理盐水能够增加血管外容量 , 降低肾脏皮质血流 。
一项单中心的研究证实 , 使用氯限制性的平衡液进行复苏能够降低AKI的发生率 , CRRT的概率也降低 。 但是多中心随机双盲试验却没有发现这种益处 。 不够这项研究因为主要面对的是手术后患者 , 且液体复苏用量较少(平均是2L) , 因此备受批评 。
血压控制
休克患者血压维持很有挑战性 。 有研究对比65-70mmHg和80-85mmHg的血压目标管理 , 发现两者之间死亡率没有差异 。 但是80-85mmHg , 如果合并慢性高血压 , 患者CRRT概率较低 。 80-85 mmHg组患者房颤发生率较高 。 因此 , 血压制定应当参照发病期的基础血压情况 , 权衡利弊 。
利尿剂
袢利尿剂在AKI无尿患者中使用较多 , 尽管没有证据表明袢利尿剂的使用有益处 。 袢利尿剂能够抑制肾髓质离子协同转运蛋白 , 降低氧需 , 减少肾脏缺血事件的发生 , 同能够避免液体过负荷 。 但是临床研究没有发现使用袢利尿剂的好处 。 因此 , KDIGO不推荐使用袢利尿剂 , 除非有液体过负荷的表现 , 或者他们的使用本身是为了调控容量 。 在AKI的早期 , 对利尿剂有反应有一定的预示作用 , 提示预后良好 , 肾小管功能保留 , 但是这种研究没被多中心研究证实 。
血糖和营养供应
AKI的患者分解代谢增加 , 需要进行肠内或肠外的应用支持 , 通常来说肠内营养更好 , 因为它感染风险较低(在同等能量供应下肠内液体需要量少) 。 AKI的患者因为病因不同、是否需要肾脏替代 , 营养供应也多种多样
关于血糖 , KDIGO建议控制在110-149mg/dl , 但是这个标准从未被研究证实 。 严格控制血糖可引起低血糖事件 , 加重病情 。
药物治疗
目前没有药物能够预防或治疗AKI 。 AKI病因各种各样 , 使用一种药物治疗AKI几乎不可能 。 此外 , AKI的发生往往在临床监测到症状、体征之前 , 治疗有延后性 , 提前干预很困难 。
AKI的患者会出现高钾血症、代谢性酸中毒、液体过负荷、尿毒症症状 。 代谢性酸中毒可以是肾脏造成的 , 也可能是低灌注原发病导致的 。 在乳酸代谢方面 , 肾脏也非常重要 。 代谢性酸中毒的治疗取决于酸中毒的严重程度 , 必须要考虑到PH值 , 酸碱变化严重程度和潜在病因 。 代谢性酸中毒可以使用碳酸氢钠或其他碱盐 。 利尿剂可以用来调控容量 。
除了以上妥协性的治疗 , 很多严重的AKI患者需要肾脏替代 。 肾脏替代时机选择有争议 。 目前能够拿到的很多回顾性研究发现 , 早期进行肾脏替代治疗有好处 。 但是这些研究对于早期的定义不同 。 因此 , 早期进行肾脏替代是否有益 , 目前众说纷纭 。
肾脏替代
目前最常用的是CRRT和IHD 。 目前KDIGO推荐CRRT和IHD相互补充 , 使用的选择取决于患者的血流动力学状态、液体状态和出血风险 , 以及医疗设备的熟悉程度、经验情况 。 目前推荐的CRRT剂量是20 to 25 mL/kg/h 。
CRRT的终止可参考以下情况1.肾功能恢复 , 能够满足机体需求;2.机体内环境改善;3.CRRT和治疗目标已经不一致;目前没有证据能够指导临床医师何时停用CRRT , 但是尿量似乎可以作为一个指标 。 在一项研究中发现 , 在没有利尿剂情况下24小时尿量>400ml/d或使用利尿剂情况下尿量达到2300ml/d,这一部分病人CRRT撤除成功率可超过80% 。
造影剂相关肾损伤
造影剂相关肾损伤(CI-AKI)是特殊的AKI类型 , 在造影剂暴露之后的数天之内肌酐水平小幅度上升 , 往往能够自陷 。 造影剂相关的肾损伤和远期、近期死亡率相关 , 有几率发生慢性肾功能不全 。 目前有研究表明造影剂引起肾损伤有被夸大的成分 。
尽管如此 , 在临床实践当中 , 仍然需要考虑到造影剂的利弊 。 造影剂相关肾损伤的首要危险因素是慢性肾功能不全 , CI-AKI在肾小球滤过率下降、蛋白尿等的时候发生率较高 。
糖尿病增加了这些患者发生CKD的风险 。 低血容量、非甾体类药物的使用同样能够加重造影剂肾损伤 。 其他的因素包括高剂量造影剂的使用、动脉造影剂的使用、多种造影剂短时间内暴露和高渗性造影剂 。
应当尽量避免造影剂的使用 , 选择非造影剂类的检查手段 。 使用碘造影剂的患者应当终止肾毒性药物的使用比如非甾体类药物 , 至少在造影剂使用24小时之前避免使用相关药物 。
应当使用低渗或等渗的造影剂 , 因为他们能够降低AKI的发生率 , 而且造影剂使用量越少越好 。 通常推荐造影剂12小时前后使用1-mL/kg/h的液体供应 , 或者造影剂前3 mL/kg/ h维持1小时 ,造影剂后1.5 mL/kg/h维持4-6小时 。 血液透析对于CI-AKI并没有帮助 。
随访问题
除了慢性肾功能不全和死亡 , AKI和心血管事件也密切相关 。 AKI患者有58%的概率出现心衰和48%的概率出现急性心梗 。 一个主要的原因就是高血压 。 之前没有合并高血压的AKI患者2年内出现高血压的概率非常大 。
目前推荐AKI的患者3个月常规随访以确定是否肾功能恶化 。 尽管肾功能恢复到基线水平 , 也应当去评估后续肾功能的发生发展情况 , 避免出现CKD 。
文章图片
推荐阅读
- 糖尿病|这根血管堵了,离死亡最近!三个预警信号,糖尿病患者尤其要注意!
- 甲状腺疾病|甲状腺疾病患者可以接种新冠疫苗吗?北京疾控释疑
- 乙肝|和乙肝患者一起吃饭到底会不会被传染?
- 北京疾控|北京疾控:甲状腺疾病患者新冠疫苗预防接种注意这些事
- 肝癌|惊艳:CAR-T实体瘤治疗又一重大突破!成功挽救晚期肝癌患者
- 尿毒症|尿毒症越来越多,医生提醒:少吃3种食物,肾病不敢找你麻烦
- 慢乙肝|【原创】慢乙肝患者这些因素会影响疾病进程?
- 肾脏|身体总是感觉乏力,不一定是因为劳累,也可能是肾脏出了问题
- 急性卡他性结膜炎|【健康提醒】阳春三月惠州万紫千红,赏花同时也要注意这5种眼病!
- 肾病综合征|肾病综合征患者复诊注意事项,关注这3点,自己也能看懂尿常规
















